Page 613 - Quimica - Undécima Edición
P. 613
13.3 Relación entre la concentración de reactivos y el tiempo 583
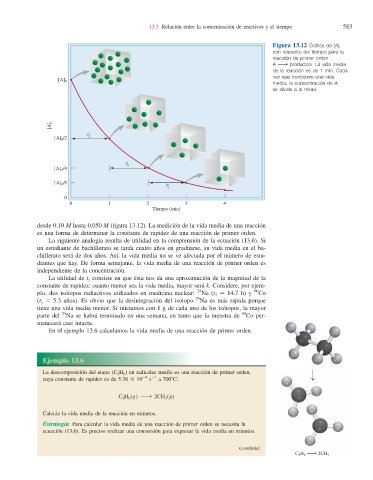
Figura 13.12 Gráfi ca de [A] t
con respecto del tiempo para la
reacción de primer orden
A ¡ productos. La vida media
de la reacción es de 1 min. Cada
vez que transcurre una vida
[A] 0
media, la concentración de A
se divide a la mitad.
[A] t
[A] 0 /2 t 1 2
[A] 0 /4 t 1 2
[A] 0 /8 t 1 2
0
0 1 2 3 4
Tiempo (min)
desde 0.10 M hasta 0.050 M (fi gura 13.12). La medición de la vida media de una reacción
es una forma de determinar la constante de rapidez de una reacción de primer orden.
La siguiente analogía resulta de utilidad en la comprensión de la ecuación (13.6). Si
un estudiante de bachillerato se tarda cuatro años en graduarse, su vida media en el ba-
chillerato será de dos años. Así, la vida media no se ve afectada por el número de estu-
diantes que hay. De forma semejante, la vida media de una reacción de primer orden es
independiente de la concentración.
La utilidad de t 1 consiste en que ésta nos da una aproximación de la magnitud de la
2
constante de rapidez: cuanto menor sea la vida media, mayor será k. Considere, por ejem-
24
60
plo, dos isótopos radiactivos utilizados en medicina nuclear: Na (t 1 5 14.7 h) y Co
2
24
(t 1 5 5.3 años). Es obvio que la desintegración del isótopo Na es más rápida porque
2
tiene una vida media menor. Si iniciamos con 1 g de cada uno de los isótopos, la mayor
24
60
parte del Na se habrá terminado en una semana, en tanto que la muestra de Co per-
manecerá casi intacta.
En el ejemplo 13.6 calculamos la vida media de una reacción de primer orden.
Ejemplo 13.6
La descomposición del etano (C 2 H 6 ) en radicales metilo es una reacción de primer orden, 8n
21
24
cuya constante de rapidez es de 5.36 3 10 s a 7008C:
C 2 H 6 (g) ¡ 2CH 3 (g)
Calcule la vida media de la reacción en minutos.
Estrategia Para calcular la vida media de una reacción de primer orden se necesita la
ecuación (13.6). Es preciso realizar una conversión para expresar la vida media en minutos.
(continúa)
C 2 H 6 ¡ 2CH 3