Page 610 - Quimica - Undécima Edición
P. 610
580 CAPÍTULO 13 Cinética química
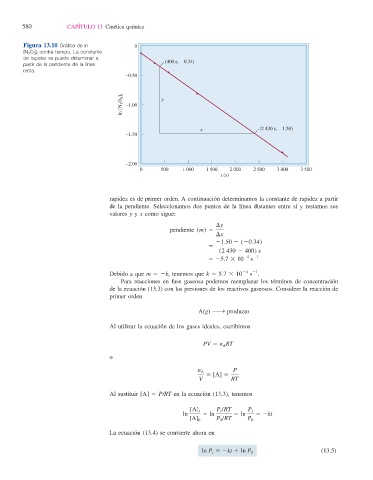
Figura 13.10 Gráfi ca de ln 0
[N 2 O 5 ] t contra tiempo. La constante
de rapidez se puede determinar a
(400 s, 0.34)
partir de la pendiente de la línea
recta.
–0.50
ln [N 2 O 5 ] t –1.00 y
x (2 430 s, 1.50)
–1.50
–2.00
0 500 1 000 1 500 2 000 2 500 3 000 3 500
t (s)
rapidez es de primer orden. A continuación determinamos la constante de rapidez a partir
de la pendiente. Seleccionamos dos puntos de la línea distantes entre sí y restamos sus
valores y y x como sigue:
¢y
pendiente (m) 5
¢x
21.50 2 (20.34)
5
(2 430 2 400) s
s
525.7 3 10 24 21
21
24
Debido a que m 5 2k, tenemos que k 5 5.7 3 10 s .
Para reacciones en fase gaseosa podemos reemplazar los términos de concentración
de la ecuación (13.3) con las presiones de los reactivos gaseosos. Considere la reacción de
primer orden
A(g) ¡ producto
Al utilizar la ecuación de los gases ideales, escribimos
PV 5 n A RT
o
n A P
5 [A] 5
V RT
Al sustituir [A] 5 P/RT en la ecuación (13.3), tenemos
P t /RT
[A] t P t
ln 5 ln 5 ln 52kt
P 0 /RT
[A] 0 P 0
La ecuación (13.4) se convierte ahora en
n l P t 52kt 1 ln P 0 1 ( ) 5 . 3