Page 608 - Quimica - Undécima Edición
P. 608
578 CAPÍTULO 13 Cinética química
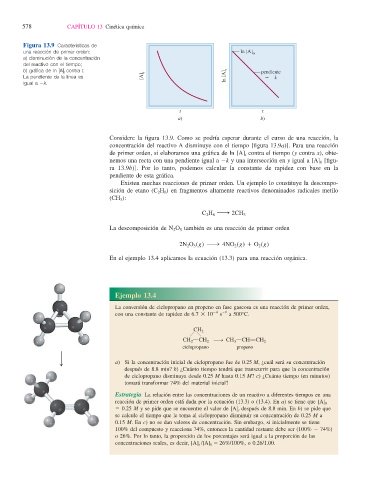
Figura 13.9 Características de
una reacción de primer orden: ln [A]
0
a) disminución de la concentración
del reactivo con el tiempo;
b) gráfi ca de ln [A] t contra t. pendiente
[A] t ln [A] t
La pendiente de la línea es k
igual a 2k.
t t
a) b)
Considere la fi gura 13.9. Como se podría esperar durante el curso de una reacción, la
concentración del reactivo A disminuye con el tiempo [fi gura 13.9a)]. Para una reacción
de primer orden, si elaboramos una gráfi ca de ln [A] t contra el tiempo (y contra x), obte-
nemos una recta con una pendiente igual a 2k y una intersección en y igual a [A] 0 [fi gu-
ra 13.9b)]. Por lo tanto, podemos calcular la constante de rapidez con base en la
pendiente de esta gráfi ca.
Existen muchas reacciones de primer orden. Un ejemplo lo constituye la descompo-
sición de etano (C 2 H 6 ) en fragmentos altamente reactivos denominados radicales metilo
(CH 3 ) :
C 2 H 6 ¡ 2CH 3
La descomposición de N 2 O 5 también es una reacción de primer orden
2N 2 O 5 (g) ¡ 4NO 2 (g) 1 O 2 (g)
En el ejemplo 13.4 aplicamos la ecuación (13.3) para una reacción orgánica.
Ejemplo 13.4
La conversión de ciclopropano en propeno en fase gaseosa es una reacción de primer orden,
21
24
con una constante de rapidez de 6.7 3 10 s a 500°C.
CH 2
D G
CH 2 OCH 2 88n CH 3 OCHPCH 2
ciclopropano propeno
a) Si la concentración inicial de ciclopropano fue de 0.25 M, ¿cuál será su concentración
88n
después de 8.8 min? b) ¿Cuánto tiempo tendrá que transcurrir para que la concentración
de ciclopropano disminuya desde 0.25 M hasta 0.15 M? c) ¿Cuánto tiempo (en minutos)
tomará transformar 74% del material inicial?
Estrategia La relación entre las concentraciones de un reactivo a diferentes tiempos en una
reacción de primer orden está dada por la ecuación (13.3) o (13.4). En a) se tiene que [A] 0
5 0.25 M y se pide que se encuentre el valor de [A] t después de 8.8 min. En b) se pide que
se calcule el tiempo que le toma al ciclopropano disminuir su concentración de 0.25 M a
0.15 M. En c) no se dan valores de concentración. Sin embargo, si inicialmente se tiene
100% del compuesto y reacciona 74%, entonces la cantidad restante debe ser (100% 2 74%)
o 26%. Por lo tanto, la proporción de los porcentajes será igual a la proporción de las
concentraciones reales, es decir, [A] t /[A] 0 5 26%/100%, o 0.26/1.00.