Page 612 - Quimica - Undécima Edición
P. 612
582 CAPÍTULO 13 Cinética química
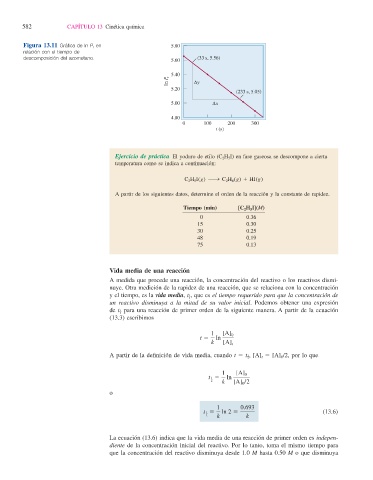
Figura 13.11 Gráfi ca de ln P t en 5.80
relación con el tiempo de
descomposición del azometano. (33 s, 5.56)
5.60
1n P t 5.40 Δy
5.20
(233 s, 5.05)
5.00 Δx
4.80
0 100 200 300
t (s)
Ejercicio de práctica El yoduro de etilo (C 2 H 5 I) en fase gaseosa se descompone a cierta
temperatura como se indica a continuación:
C 2 H 5 I(g) ¡ C 2 H 4 (g) 1 HI(g)
A partir de los siguientes datos, determine el orden de la reacción y la constante de rapidez.
Tiempo (min) [C 2 H 5 I](M)
0 0.36
15 0.30
30 0.25
48 0.19
75 0.13
Vida media de una reacción
A medida que procede una reacción, la concentración del reactivo o los reactivos dismi-
nuye. Otra medición de la rapidez de una reacción, que se relaciona con la concentración
y el tiempo, es la vida media, t 1 , que es el tiempo requerido para que la concentración de
2
un reactivo disminuya a la mitad de su valor inicial. Podemos obtener una expresión
de t 1 para una reacción de primer orden de la siguiente manera. A partir de la ecuación
2
(13.3) escribimos
1 [A] 0
t 5 ln
k [A] t
A partir de la defi nición de vida media , cuando t 5 t 1 , [A] t 5 [A] 0 /2, por lo que
2
1 [A] 0
t 5 ln
1
2 k [A] 0 /2
o
1 0.693
t 5 ln 2 5 1 ( ) 6 . 3
1
2 k k
La ecuación (13.6) indica que la vida media de una reacción de primer orden es indepen-
diente de la concentración inicial del reactivo. Por lo tanto, toma el mismo tiempo para
que la concentración del reactivo disminuya desde 1.0 M hasta 0.50 M o que disminuya