Page 620 - Quimica - Undécima Edición
P. 620
590 CAPÍTULO 13 Cinética química
13.4 Constantes de rapidez y su dependencia de la
energía de activación y de la temperatura
Constante de rapidez Con muy pocas excepciones, la rapidez de las reacciones aumenta al incrementar la tem-
peratura. Por ejemplo, el tiempo que se requiere para cocer un huevo en agua es mucho
menor si la “reacción” se lleva a cabo a 100°C (unos 10 min) que a 80°C (cerca de 30
min). Por lo contrario, una forma efectiva de conservar alimentos consiste en almacenar-
los a temperaturas bajo cero, para que disminuya la rapidez de descomposición bacteriana.
En la fi gura 13.15 se ilustra un ejemplo típico de la relación entre la constante de rapidez
de una reacción y la temperatura. Para explicar este comportamiento es necesario pregun-
Temperatura
tarnos cómo se inician las reacciones.
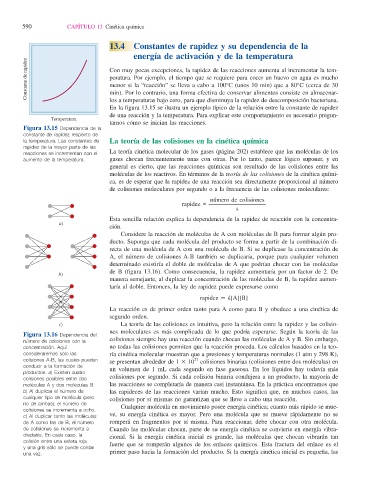
Figura 13.15 Dependencia de la
constante de rapidez respecto de
la temperatura. Las constantes de La teoría de las colisiones en la cinética química
rapidez de la mayor parte de las
reacciones se incrementan con el La teoría cinética molecular de los gases (página 202) establece que las moléculas de los
aumento de la temperatura. gases chocan frecuentemente unas con otras. Por lo tanto, parece lógico suponer, y en
general es cierto, que las reacciones químicas son resultado de las colisiones entre las
moléculas de los reactivos . En términos de la teoría de las colisiones de la cinética quími-
ca , es de esperar que la rapidez de una reacción sea directamente proporcional al número
de colisiones moleculares por segundo o a la frecuencia de las colisiones moleculares:
número de colisiones
rapidez ~
s
Esta sencilla relación explica la dependencia de la rapidez de reacción con la concentra-
a)
ción.
Considere la reacción de moléculas de A con moléculas de B para formar algún pro-
ducto. Suponga que cada molécula del producto se forma a partir de la combinación di-
recta de una molécula de A con una molécula de B. Si se duplicase la concentración de
A, el número de colisiones A-B también se duplicaría, porque para cualquier volumen
determinado existiría el doble de moléculas de A que podrían chocar con las moléculas
de B (fi gura 13.16). Como consecuencia, la rapidez aumentaría por un factor de 2. De
b)
manera semejante, al duplicar la concentración de las moléculas de B, la rapidez aumen-
taría al doble. Entonces, la ley de rapidez puede expresarse como
rapidez 5 k[A][B]
La reacción es de primer orden tanto para A como para B y obedece a una cinética de
segundo orden .
c) La teoría de las colisiones es intuitiva, pero la relación entre la rapidez y las colisio-
nes moleculares es más complicada de lo que podría esperarse. Según la teoría de las
Figura 13.16 Dependencia del
número de colisiones con la colisiones siempre hay una reacción cuando chocan las moléculas de A y B. Sin embargo,
concentración. Aquí no todas las colisiones permiten que la reacción proceda. Los cálculos basados en la teo-
consideraremos sólo las ría cinética molecular muestran que a presiones y temperaturas normales (1 atm y 298 K),
27
colisiones A-B, las cuales puedan se presentan alrededor de 1 3 10 colisiones binarias (colisiones entre dos moléculas) en
conducir a la formación de un volumen de 1 mL cada segundo en fase gaseosa. En los líquidos hay todavía más
productos. a) Existen cuatro
colisiones posibles entre dos colisiones por segundo. Si cada colisión binaria condujera a un producto, la mayoría de
moléculas A y dos moléculas B. las reacciones se completaría de manera casi instantánea. En la práctica encontramos que
b) Al duplicar el número de las rapideces de las reacciones varían mucho. Esto signifi ca que, en muchos casos, las
cualquier tipo de molécula (pero colisiones por sí mismas no garantizan que se lleve a cabo una reacción.
no de ambas), el número de Cualquier molécula en movimiento posee energía cinética ; cuanto más rápido se mue-
colisiones se incrementa a ocho.
c) Al duplicar tanto las moléculas ve, su energía cinética es mayor. Pero una molécula que se mueve rápidamente no se
de A como las de B, el número romperá en fragmentos por sí misma. Para reaccionar, debe chocar con otra molécula.
de colisiones se incrementa a Cuando las moléculas chocan, parte de su energía cinética se convierte en energía vibra-
dieciséis. En cada caso, la cional . Si la energía cinética inicial es grande, las moléculas que chocan vibrarán tan
colisión entre una esfera roja fuerte que se romperán algunos de los enlaces químicos. Esta fractura del enlace es el
y una gris sólo se puede contar
una vez. primer paso hacia la formación del producto. Si la energía cinética inicial es pequeña, las