Page 623 - Quimica - Undécima Edición
P. 623
13.4 Constantes de rapidez y su dependencia de la energía de activación y de la temperatura 593
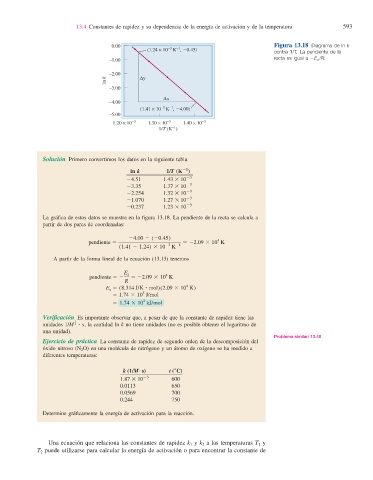
0.00 Figura 13.18 Diagrama de ln k
–3 –1
(1.24 × 10 K , 0.45)
contra 1/T. La pendiente de la
recta es igual a 2E a /R.
–1.00
–2.00
1n k Δy
–3.00
Δx
–4.00
–3 –1
(1.41 × 10 K , 4.00)
–5.00
1.20 × 10 –3 1.30 × 10 –3 1.40 × 10 –3
–1
1/T (K )
Solución Primero convertimos los datos en la siguiente tabla
1
ln k 1/T (K )
4.51 1.43 10 3
3.35 1.37 10 3
2.254 1.32 10 3
1.070 1.27 10 3
0.237 1.23 10 3
La gráfi ca de estos datos se muestra en la fi gura 13.18. La pendiente de la recta se calcula a
partir de dos pares de coordenadas:
24.00 2 (20.45)
4
pendiente 5 522.09 3 10 K
23
(1.41 2 1.24) 3 10 K 21
A partir de la forma lineal de la ecuación (13.13) tenemos
E a 4
pendiente 52 522.09 3 10 K
R
4
E a 5 (8.314 J/K ? mol)(2.09 3 10 K)
5
5 1.74 3 10 J/mol
2
5 1.74 3 10 kJ/mol
Verifi cación Es importante observar que, a pesar de que la constante de rapidez tiene las
1
unidades 1/M ? s, la cantidad ln k no tiene unidades (no es posible obtener el logaritmo de
2
una unidad).
Problema similar: 13.40
Ejercicio de práctica La constante de rapidez de segundo orden de la descomposición del
óxido nitroso (N 2 O) en una molécula de nitrógeno y un átomo de oxígeno se ha medido a
diferentes temperaturas:
k (1/M s) t (°C)
1.87 10 3 600
0.0113 650
0.0569 700
0.244 750
Determine gráfi camente la energía de activación para la reacción.
Una ecuación que relaciona las constantes de rapidez k 1 y k 2 a las temperaturas T 1 y
T 2 puede utilizarse para calcular la energía de activación o para encontrar la constante de