Page 621 - Quimica - Undécima Edición
P. 621
13.4 Constantes de rapidez y su dependencia de la energía de activación y de la temperatura 591
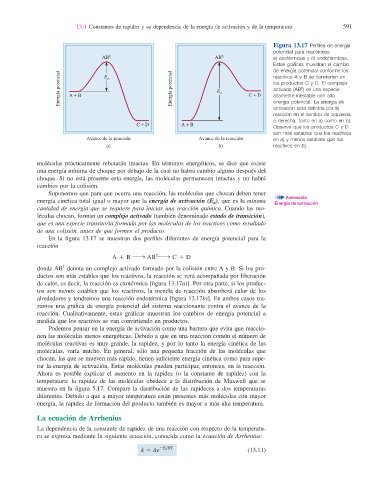
Figura 13.17 Perfi les de energía
potencial para reacciones
AB ‡ AB ‡ a) exotérmicas y b) endotérmicas.
Estas gráfi cas muestran el cambio
de energía potencial conforme los
Energía potencial A + B Energía potencial E a C + D los productos C y D. El complejo
E
reactivos A y B se convierten en
a
‡
activado (AB ) es una especie
altamente inestable con alta
energía potencial. La energía de
activación está defi nida por la
reacción en el sentido de izquierda
a derecha, tanto en a) como en b).
C + D A + B
Observe que los productos C y D
son más estables que los reactivos
Avance de la reacción Avance de la reacción en a) y menos estables que los
a) b) reactivos en b).
moléculas prácticamente rebotarán intactas. En términos energéticos, se dice que existe
una energía mínima de choque por debajo de la cual no habrá cambio alguno después del
choque. Si no está presente esta energía, las moléculas permanecen intactas y no habrá
cambios por la colisión.
Suponemos que para que ocurra una reacción, las moléculas que chocan deben tener
Animación
energía cinética total igual o mayor que la energía de activación (E a ) , que es la mínima
Energía de activación
cantidad de energía que se requiere para iniciar una reacción química. Cuando las mo-
léculas chocan, forman un complejo activado (también denominado estado de transición ),
que es una especie transitoria formada por las moléculas de los reactivos como resultado
de una colisión, antes de que formen el producto.
En la fi gura 13.17 se muestran dos perfi les diferentes de energía potencial para la
reacción
‡
A 1 B ¡ AB ¡ C 1 D
‡
donde AB denota un complejo activado formado por la colisión entre A y B. Si los pro-
ductos son más estables que los reactivos, la reacción se verá acompañada por liberación
de calor, es decir, la reacción es exotérmica [fi gura 13.17a)]. Por otra parte, si los produc-
tos son menos estables que los reactivos, la mezcla de reacción absorberá calor de los
alrededores y tendremos una reacción endotérmica [fi gura 13.17b)]. En ambos casos tra-
zamos una gráfi ca de energía potencial del sistema reaccionante contra el avance de la
reacción. Cualitativamente, estas gráfi cas muestran los cambios de energía potencial a
medida que los reactivos se van convirtiendo en productos.
Podemos pensar en la energía de activación como una barrera que evita que reaccio-
nen las moléculas menos energéticas. Debido a que en una reacción común el número de
moléculas reactivas es muy grande, la rapidez, y por lo tanto la energía cinética de las
moléculas, varía mucho. En general, sólo una pequeña fracción de las moléculas que
chocan, las que se mueven más rápido, tienen sufi ciente energía cinética como para supe-
rar la energía de activación. Estas moléculas pueden participar, entonces, en la reacción.
Ahora es posible explicar el aumento en la rapidez (o la constante de rapidez) con la
temperatura: la rapidez de las moléculas obedece a la distribución de Maxwell que se
muestra en la fi gura 5.17. Compare la distribución de las rapideces a dos temperaturas
diferentes. Debido a que a mayor temperatura están presentes más moléculas con mayor
energía, la rapidez de formación del producto también es mayor a más alta temperatura.
La ecuación de Arrhenius
La dependencia de la constante de rapidez de una reacción con respecto de la temperatu-
ra se expresa mediante la siguiente ecuación, conocida como la ecuación de Arrhenius :
k 5 Ae 2E a /RT ) 1 1 . 3 1 (