Page 67 - Libro Hipertextos Quimica 2
P. 67
Componente: Procesos físicos
1.1.1 Propiedades físicas
400
En estado puro, los alcanos son incoloros, presentan una Sólidos • • •
densidad menor que la del agua y debido a su naturaleza 300 • • •
apolar, son insolubles en agua, pero solubles en solventes • • •
orgánicos como el tetracloruro de carbono o el benceno. 200 • • Líquidos
En cuanto al estado de agregación, a temperatura am- Punto de ebullición °C 100 • • •
biente, los cuatro primeros alcanos (metano, etano, pro- • •
pano y butano), son gases; del pentano al heptadecano son 0 •
líquidos, mientras que cadenas mayores se encuentran 100 • Gases
como sólidos.
•
200
En general, a medida que aumenta el número de carbonos 2 4 6 8 10 12 14 16 18 20
presentes (es decir, el peso molecular), se observa un au- Número de átomos de carbono
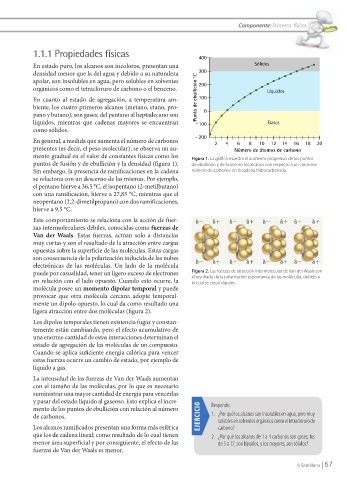
mento gradual en el valor de constantes físicas como los Figura 1. La gráfi ca muestra el aumento progresivo de los puntos
puntos de fusión y de ebullición y la densidad (fi gura 1). de ebullición y de fusión en los alcanos con respecto a un creciente
Sin embargo, la presencia de ramifi caciones en la cadena número de carbonos en la cadena hidrocarbonada.
se relaciona con un descenso de las mismas. Por ejemplo,
el pentano hierve a 36,5 °C, el isopentano (2-metilbutano)
con una ramifi cación, hierve a 27,85 °C, mientras que el
neopentano (2,2-dimetilpropano) con dos ramifi caciones,
hierve a 9,5 °C.
Este comportamiento se relaciona con la acción de fuer-
zas intermoleculares débiles, conocidas como fuerzas de
Van der Waals. Estas fuerzas, actúan solo a distancias
muy cortas y son el resultado de la atracción entre cargas
opuestas sobre la superfi cie de las moléculas. Estas cargas
son consecuencia de la polarización inducida de las nubes
electrónicas de las moléculas. Un lado de la molécula
puede por casualidad, tener un ligero exceso de electrones Figura 2. Las fuerzas de atracción intermolecular de Van der Waals son
el resultado de la polarización espontánea de las moléculas, debido a
en relación con el lado opuesto. Cuando esto ocurre, la lo cual se crean dipolos.
molécula posee un momento dipolar temporal y puede
provocar que otra molécula cercana adopte temporal-
mente un dipolo opuesto, lo cual da como resultado una
ligera atracción entre dos moléculas (fi gura 2).
Los dipolos temporales tienen existencia fugaz y constan-
temente están cambiando, pero el efecto acumulativo de
una enorme cantidad de estas interacciones determinan el
estado de agregación de las moléculas de un compuesto.
Cuando se aplica sufi ciente energía calórica para vencer
estas fuerzas ocurre un cambio de estado, por ejemplo de
líquido a gas.
La intensidad de las fuerzas de Van der Waals aumentan
con el tamaño de las moléculas, por lo que es necesario
suministrar una mayor cantidad de energía para vencerlas
y pasar del estado líquido al gaseoso. Esto explica el incre-
mento de los puntos de ebullición con relación al número Responde:
de carbonos. EJERCICIO 1. ¿Por qué los alcanos son insolubles en agua, pero muy
solubles en solventes orgánicos como el tetracloruro de
Los alcanos ramifi cados presentan una forma más esférica carbono?
que los de cadena lineal; como resultado de lo cual tienen 2. ¿Por qué los alcanos de 1 a 4 carbonos son gases, los
menor área superfi cial y por consiguiente, el efecto de las de 5 a 17, son líquidos, y los mayores, son sólidos?
fuerzas de Van der Waals es menor.
© Santillana 67
QUIM11-U3(64-97).indd 67 22/12/09 10:02