Page 597 - Quimica - Undécima Edición
P. 597
13.1 La rapidez de una reacción 567
t 1
Absorción t t 2 3
300 400 500 600
Longitud de onda (nm)
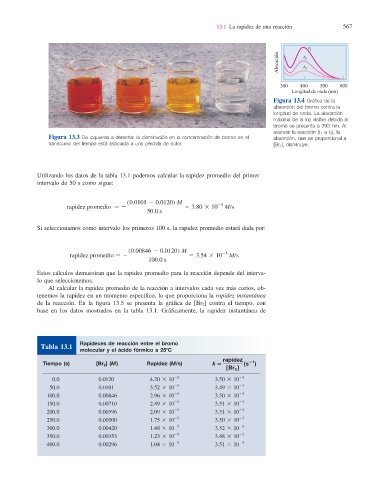
Figura 13.4 Gráfi ca de la
absorción del bromo contra la
longitud de onda. La absorción
máxima de la luz visible debida al
bromo se presenta a 393 nm. Al
avanzar la reacción (t 1 a t 3 ), la
Figura 13.3 De izquierda a derecha: la disminución en la concentración de bromo en el absorción, que es proporcional a
transcurso del tiempo está asociada a una pérdida de color. [Br 2 ], disminuye.
Utilizando los datos de la tabla 13.1 podemos calcular la rapidez promedio del primer
intervalo de 50 s como sigue:
(0.0101 2 0.0120) M
25
rapidez promedio 52 5 3.80 3 10 M/s
50.0 s
Si seleccionamos como intervalo los primeros 100 s, la rapidez promedio estará dada por:
(0.00846 2 0.0120) M
25
rapidez promedio 52 5 3.54 3 10 M/s
100.0 s
Estos cálculos demuestran que la rapidez promedio para la reacción depende del interva-
lo que seleccionemos.
Al calcular la rapidez promedio de la reacción a intervalos cada vez más cortos, ob-
tenemos la rapidez en un momento específi co , lo que proporciona la rapidez instantánea
de la reacción . En la fi gura 13.5 se presenta la gráfi ca de [Br 2 ] contra el tiempo, con
base en los datos mostrados en la tabla 13.1. Gráfi camente, la rapidez instantánea de
Rapideces de reacción entre el bromo
Tabla 13.1
molecular y el ácido fórmico a 258C
rapidez
Tiempo (s) [Br 2 ] (M) Rapidez (M/s) k 5 (s 21 )
[Br 2 ]
0.0 0.0120 4.20 3 10 25 3.50 3 10 23
50.0 0.0101 3.52 3 10 25 3.49 3 10 23
100.0 0.00846 2.96 3 10 25 3.50 3 10 23
150.0 0.00710 2.49 3 10 25 3.51 3 10 23
200.0 0.00596 2.09 3 10 25 3.51 3 10 23
250.0 0.00500 1.75 3 10 25 3.50 3 10 23
300.0 0.00420 1.48 3 10 25 3.52 3 10 23
350.0 0.00353 1.23 3 10 25 3.48 3 10 23
400.0 0.00296 1.04 3 10 25 3.51 3 10 23