Page 600 - Quimica - Undécima Edición
P. 600
570 CAPÍTULO 13 Cinética química
Descomposición del peróxido de hidrógeno
Si uno de los productos o reactivos es un gas, podemos utilizar el manómetro para encon-
trar la rapidez de la reacción. Considere la descomposición del peróxido de hidrógeno a
20°C:
2H 2 O 2 (ac) ¡ 2H 2 O(l) 1 O 2 (g)
En este caso, la rapidez de descomposición se determina midiendo la rapidez de formación
de oxígeno mediante un manómetro (fi gura 13.7). La presión de oxígeno puede convertir-
se fácilmente en concentración utilizando la ecuación de los gases ideales :
8n
PV 5 nRT
o
n
P 5 RT 5 [O 2 ]RT
V
donde n/V da la molaridad del oxígeno gaseoso. Al reacomodar la ecuación, obtenemos
2H 2 O 2 ¡ 2H 2 O 1 O 2
1
[ O 2 ] 5 P
RT
La rapidez de la reacción, que está dada por la rapidez de producción de oxígeno, ahora
puede escribirse como
¢[O 2 ] 1 ¢P
rapidez 5 5
¢t RT ¢t
En la fi gura 13.8 se muestra el aumento de la presión del oxígeno en el tiempo y la de-
terminación de la rapidez instantánea a 400 min. Para expresar la rapidez en las unidades
120
100
80
P (mmHg) 60 Pendiente = 0.12 mmHg/min
40
20
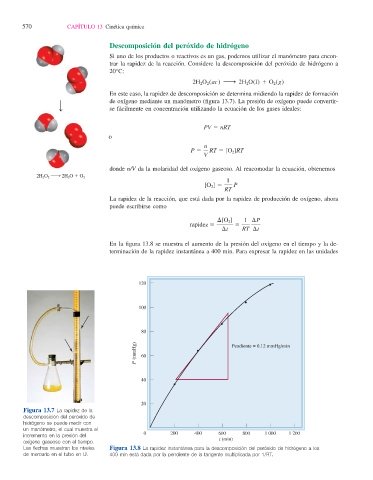
Figura 13.7 La rapidez de la
descomposición del peróxido de
hidrógeno se puede medir con
un manómetro, el cual muestra el
incremento en la presión del 0 200 400 600 800 1 000 1 200
t (min)
oxígeno gaseoso con el tiempo.
Las fl echas muestran los niveles Figura 13.8 La rapidez instantánea para la descomposición del peróxido de hidrógeno a los
de mercurio en el tubo en U. 400 min está dada por la pendiente de la tangente multiplicada por 1/RT.