Page 599 - Quimica - Undécima Edición
P. 599
13.1 La rapidez de una reacción 569
5.00 3 10 –5
4.00 3 10 –5
Rapidez (M/s) 3.00 3 10 –5
–5
2.00 3 10
1.00 3 10 –5
0 0.00200 0.00600 0.0100 0.0140
[Br ] (M)
2
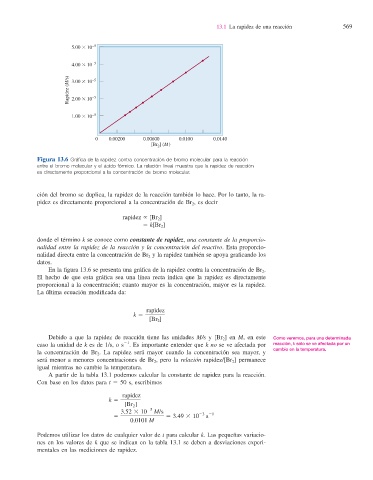
Figura 13.6 Gráfi ca de la rapidez contra concentración de bromo molecular para la reacción
entre el bromo molecular y el ácido fórmico. La relación lineal muestra que la rapidez de reacción
es directamente proporcional a la concentración de bromo molecular.
ción del bromo se duplica, la rapidez de la reacción también lo hace. Por lo tanto, la ra-
pidez es directamente proporcional a la concentración de Br 2 , es decir
rapidez ~ [Br 2 ]
5 k[Br 2 ]
donde el término k se conoce como constante de rapidez , una constante de la proporcio-
nalidad entre la rapidez de la reacción y la concentración del reactivo . Esta proporcio-
nalidad directa entre la concentración de Br 2 y la rapidez también se apoya grafi cando los
datos.
En la fi gura 13.6 se presenta una gráfi ca de la rapidez contra la concentración de Br 2 .
El hecho de que esta gráfi ca sea una línea recta indica que la rapidez es directamente
proporcional a la concentración; cuanto mayor es la concentración, mayor es la rapidez.
La última ecuación modifi cada da:
rapidez
k 5
[Br 2 ]
Debido a que la rapidez de reacción tiene las unidades M/s y [Br 2 ] en M, en este Como veremos, para una determinada
21
caso la unidad de k es de 1/s, o s . Es importante entender que k no se ve afectada por reacción, k sólo se ve afectada por un
cambio en la temperatura.
la concentración de Br 2 . La rapidez será mayor cuando la concentración sea mayor, y
será menor a menores concentraciones de Br 2 , pero la relación rapidez/[Br 2 ] permanece
igual mientras no cambie la temperatura.
A partir de la tabla 13.1 podemos calcular la constante de rapidez para la reacción.
Con base en los datos para t 5 50 s, escribimos
rapidez
k 5
[Br 2 ]
25
3.52 3 10 M/s
23 21
5 5 3.49 3 10 s
0.0101 M
Podemos utilizar los datos de cualquier valor de t para calcular k. Las pequeñas variacio-
nes en los valores de k que se indican en la tabla 13.1 se deben a desviaciones experi-
mentales en las mediciones de rapidez.