Page 598 - Quimica - Undécima Edición
P. 598
568 CAPÍTULO 13 Cinética química
0.0120
0.0100
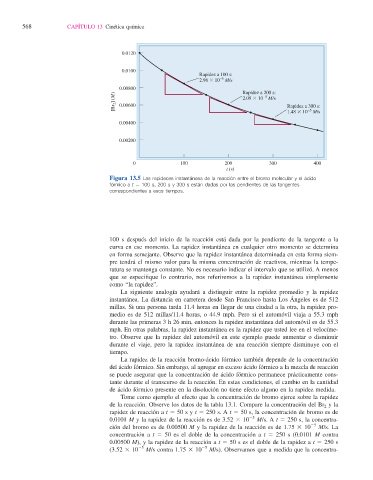
Rapidez a 100 s:
–5
2.96 3 10 M/s
0.00800 Rapidez a 200 s:
[Br 2 ] (M) 0.00600 2.09 3 10 M/s Rapidez a 300 s:
–5
–5
1.48 3 10 M/s
0.00400
0.00200
0 100 200 300 400
t (s)
Figura 13.5 Las rapideces instantáneas de la reacción entre el bromo molecular y el ácido
fórmico a t 5 100 s, 200 s y 300 s están dadas por las pendientes de las tangentes
correspondientes a esos tiempos.
100 s después del inicio de la reacción está dada por la pendiente de la tangente a la
curva en ese momento. La rapidez instantánea en cualquier otro momento se determina
en forma semejante. Observe que la rapidez instantánea determinada en esta forma siem-
pre tendrá el mismo valor para la misma concentración de reactivos, mientras la tempe-
ratura se mantenga constante. No es necesario indicar el intervalo que se utilizó. A menos
que se especifi que lo contrario, nos referiremos a la rapidez instantánea simplemente
como “la rapidez”.
La siguiente analogía ayudará a distinguir entre la rapidez promedio y la rapidez
instantánea. La distancia en carretera desde San Francisco hasta Los Ángeles es de 512
millas. Si una persona tarda 11.4 horas en llegar de una ciudad a la otra, la rapidez pro-
medio es de 512 millas/11.4 horas, o 44.9 mph. Pero si el automóvil viaja a 55.3 mph
durante las primeras 3 h 26 min, entonces la rapidez instantánea del automóvil es de 55.3
mph. En otras palabras, la rapidez instantánea es la rapidez que usted lee en el velocíme-
tro. Observe que la rapidez del automóvil en este ejemplo puede aumentar o disminuir
durante el viaje, pero la rapidez instantánea de una reacción siempre disminuye con el
tiempo.
La rapidez de la reacción bromo-ácido fórmico también depende de la concentración
del ácido fórmico. Sin embargo, al agregar en exceso ácido fórmico a la mezcla de reacción
se puede asegurar que la concentración de ácido fórmico permanece prácticamente cons-
tante durante el transcurso de la reacción. En estas condiciones, el cambio en la cantidad
de ácido fórmico presente en la disolución no tiene efecto alguno en la rapidez medida.
Tome como ejemplo el efecto que la concentración de bromo ejerce sobre la rapidez
de la reacción. Observe los datos de la tabla 13.1. Compare la concentración del Br 2 y la
rapidez de reacción a t 5 50 s y t 5 250 s. A t 5 50 s, la concentración de bromo es de
25
0.0101 M y la rapidez de la reacción es de 3.52 3 10 M/s. A t 5 250 s, la concentra-
25
ción del bromo es de 0.00500 M y la rapidez de la reacción es de 1.75 3 10 M/s. La
concentración a t 5 50 es el doble de la concentración a t 5 250 s (0.0101 M contra
0.00500 M), y la rapidez de la reacción a t 5 50 s es el doble de la rapidez a t 5 250 s
25
25
(3.52 3 10 M/s contra 1.75 3 10 M/s). Observamos que a medida que la concentra-