Page 596 - Quimica - Undécima Edición
P. 596
566 CAPÍTULO 13 Cinética química
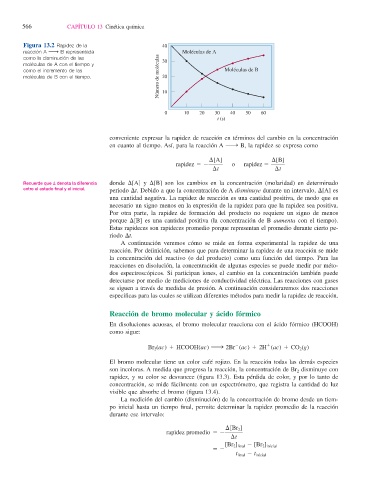
Figura 13.2 Rapidez de la 40
reacción A ¡ B representada Moléculas de A
como la disminución de las 30
moléculas de A con el tiempo y
como el incremento de las Moléculas de B
moléculas de B con el tiempo. Número de moléculas 20
10
0 10 20 30 40 50 60
t (s)
conveniente expresar la rapidez de reacción en términos del cambio en la concentración
en cuanto al tiempo. Así, para la reacción A ¡ B, la rapidez se expresa como
¢[A] ¢[B]
rapidez 52 o rapidez 5
¢t ¢t
Recuerde que D denota la diferencia donde D[A] y D[B] son los cambios en la concentración (molaridad) en determinado
entre el estado fi nal y el inicial. periodo Dt. Debido a que la concentración de A disminuye durante un intervalo, D[A] es
una cantidad negativa. La rapidez de reacción es una cantidad positiva, de modo que es
necesario un signo menos en la expresión de la rapidez para que la rapidez sea positiva.
Por otra parte, la rapidez de formación del producto no requiere un signo de menos
porque D[B] es una cantidad positiva (la concentración de B aumenta con el tiempo).
Estas rapideces son rapideces promedio porque representan el promedio durante cierto pe-
riodo Dt.
A continuación veremos cómo se mide en forma experimental la rapidez de una
reacción. Por defi nición, sabemos que para determinar la rapidez de una reacción se mide
la concentración del reactivo (o del producto) como una función del tiempo. Para las
reacciones en disolución, la concentración de algunas especies se puede medir por méto-
dos espectroscópicos . Si participan iones, el cambio en la concentración también puede
detectarse por medio de mediciones de conductividad eléctrica . Las reacciones con gases
se siguen a través de medidas de presión. A continuación consideraremos dos reacciones
específi cas para las cuales se utilizan diferentes métodos para medir la rapidez de reacción.
Reacción de bromo molecular y ácido fórmico
En disoluciones acuosas, el bromo molecular reacciona con el ácido fórmico (HCOOH)
como sigue:
2
1
Br 2 (ac) 1 HCOOH(ac) ¡ 2Br (ac) 1 2H (ac) 1 CO 2 (g)
El bromo molecular tiene un color café rojizo. En la reacción todas las demás especies
son incoloras. A medida que progresa la reacción, la concentración de Br 2 disminuye con
rapidez, y su color se desvanece (fi gura 13.3). Esta pérdida de color, y por lo tanto de
concentración, se mide fácilmente con un espectrómetro, que registra la cantidad de luz
visible que absorbe el bromo (fi gura 13.4).
La medición del cambio (disminución) de la concentración de bromo desde un tiem-
po inicial hasta un tiempo fi nal, permite determinar la rapidez promedio de la reacción
durante ese intervalo:
¢[Br 2 ]
rapidez promedio 52
¢t
[Br 2 ] final 2 [Br 2 ] inicial
52
t final 2 t inicial