Page 559 - Quimica - Undécima Edición
P. 559
12.4 Efecto de la temperatura en la solubilidad 529
12.4 Efecto de la temperatura en la solubilidad
Recuerde que la solubilidad se defi ne como la máxima cantidad de un soluto que se pue-
de disolver en determinada cantidad de un disolvente a una temperatura específi ca. La
temperatura afecta la solubilidad de la mayor parte de las sustancias. En esta sección
analizaremos el efecto de la temperatura sobre la solubilidad de sólidos y gases.
Solubilidad de los sólidos y la temperatura
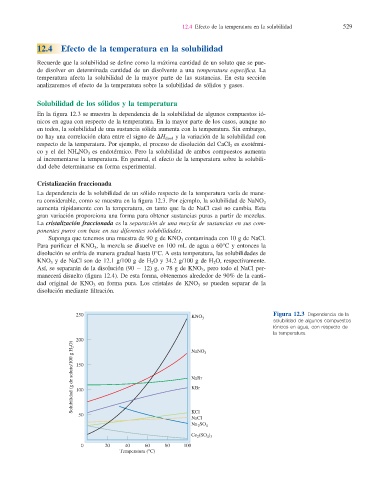
En la fi gura 12.3 se muestra la dependencia de la solubilidad de algunos compuestos ió-
nicos en agua con respecto de la temperatura. En la mayor parte de los casos, aunque no
en todos, la solubilidad de una sustancia sólida aumenta con la temperatura. Sin embargo,
no hay una correlación clara entre el signo de DH disol y la variación de la solubilidad con
respecto de la temperatura. Por ejemplo, el proceso de disolución del CaCl 2 es exotérmi-
co y el del NH 4 NO 3 es endotérmico. Pero la solubilidad de ambos compuestos aumenta
al incrementarse la temperatura. En general, el efecto de la temperatura sobre la solubili-
dad debe determinarse en forma experimental.
Cristalización fraccionada
La dependencia de la solubilidad de un sólido respecto de la temperatura varía de mane-
ra considerable, como se muestra en la fi gura 12.3. Por ejemplo, la solubilidad de NaNO 3
aumenta rápidamente con la temperatura, en tanto que la de NaCl casi no cambia. Esta
gran variación proporciona una forma para obtener sustancias puras a partir de mezclas.
La cristalización fraccionada es la separación de una mezcla de sustancias en sus com-
ponentes puros con base en sus diferentes solubilidades.
Suponga que tenemos una muestra de 90 g de KNO 3 contaminada con 10 g de NaCl.
Para purifi car el KNO 3 , la mezcla se disuelve en 100 mL de agua a 60°C y entonces la
disolución se enfría de manera gradual hasta 0°C. A esta temperatura, las solubilidades de
KNO 3 y de NaCl son de 12.1 g/100 g de H 2 O y 34.2 g/100 g de H 2 O, respectivamente.
Así, se separarán de la disolución (90 2 12) g, o 78 g de KNO 3 , pero todo el NaCl per-
manecerá disuelto (fi gura 12.4). De esta forma, obtenemos alrededor de 90% de la canti-
dad original de KNO 3 en forma pura. Los cristales de KNO 3 se pueden separar de la
disolución mediante fi ltración.
250 KNO Figura 12.3 Dependencia de la
3
solubilidad de algunos compuestos
iónicos en agua, con respecto de
la temperatura.
200 NaNO 3
Solubilidad (g de soluto/100 g H 2 O) 150 NaBr
KBr
100
50 KCl
NaCl
Na SO 4
2
Ce (SO )
4 3
2
0 20 40 60 80 100
Temperatura (°C)