Page 168 - Libro Hipertextos Quimica 1
P. 168
Los gases
1 Señala con una ✗ los enunciados que son ciertos: 5 A continuación se muestran los pesos moleculares
a) Si la presión de un gas se duplica su volumen y las densidades de algunos gases.
se reduce a la mitad, cuando la presión es cons- Gas Peso molecular Densidad (g/L)
tante.
b) El aumento de la temperatura de un gas oca- H 2 2,0 0,090
siona un mayor movimiento de las moléculas NH 3 17,0 0,760
que lo conforman.
HCN 27,0 1,21
c) El número de moléculas de un gas disminuye
al decrecer la temperatura. H S 34,0 1,52
2
d) Al comprimir un gas la energía cinética de sus CO 2 44,0 1,96
moléculas disminuye. SO 2 64,0 2,86
e) Volúmenes iguales de hidrógeno y oxígeno Cl 71,0 3,17
contienen diferente número de moléculas, a las 2
mismas condiciones de temperatura y presión. Responde:
f) La presión que ejercen las moléculas de un gas a) ¿Qué relación existe entre la densidad y el peso
sobre las paredes del recipiente depende del molecular de los gases?
número de moles presentes. b) ¿Qué expresión matemática de las leyes de los
2 En tu cuaderno completa los siguientes enuncia- gases relaciona estas dos propiedades?
dos: 6 Observa los siguientes dibujos:
a) Las magnitudes que defi nen el estado de un gas
son…
b) La ley de Boyle plantea que…
c) La ley de Charles plantea que…
3 Consulta las aplicaciones de los siguientes gases en
la vida diaria:
a) Neón e) Hidrógeno
b) Nitrógeno f) Propano
c) Cloro g) Helio
d) Oxígeno h) Amoníaco
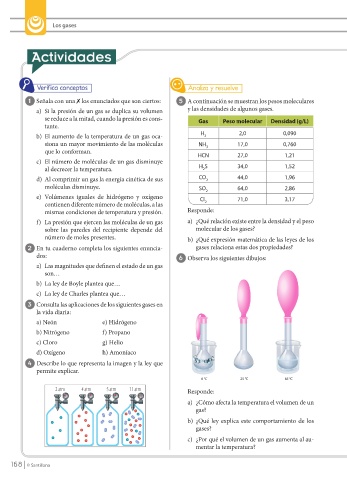
4 Describe lo que representa la imagen y la ley que
permite explicar.
0 °C 25 °C 85 °C
2 atm 4 atm 5 atm 11 atm Responde:
a) ¿Cómo afecta la temperatura el volumen de un
gas?
b) ¿Qué ley explica este comportamiento de los
gases?
c) ¿Por qué el volumen de un gas aumenta al au-
mentar la temperatura?
168
168 © Santillana
QUIM10-U4(146-171).indd 168 1/12/09 14:16