Page 566 - Quimica - Undécima Edición
P. 566
536 CAPÍTULO 12 Propiedades físicas de las disoluciones
800 donde P A y P B son las presiones parciales de los componentes A y B de la disolución; P° A
P = P benceno + P tolueno y P° B son las presiones de vapor de las sustancias puras y X A y X B son sus fracciones
T
molares. La presión total está dada por la ley de Dalton de las presiones parciales (vea la
600 sección 5.6):
Presión (mmHg) 400 P benceno o P T 5 P A 1 P B
200 P tolueno P T 5 X A P° A 1 X B P° B
Por ejemplo, el benceno y el tolueno son volátiles, tienen estructuras similares y, por lo
tanto, fuerzas intermoleculares semejantes:
0.0 0.2 0.4 0.6 0.8 1.0
X benceno CH 3
A
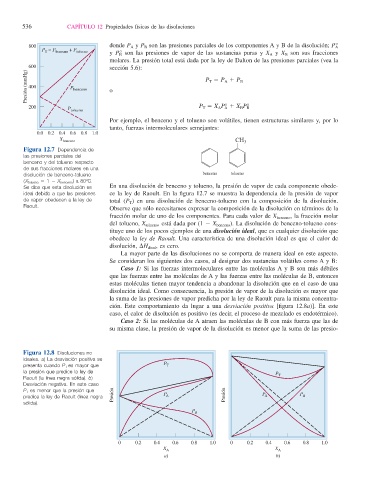
Figura 12.7 Dependencia de
las presiones parciales del
benceno y del tolueno respecto
de sus fracciones molares en una
disolución de benceno-tolueno benceno tolueno
(X tolueno 5 1 2 X benceno ) a 80ºC.
Se dice que esta disolución es En una disolución de benceno y tolueno, la presión de vapor de cada componente obede-
ideal debido a que las presiones ce la ley de Raoult. En la fi gura 12.7 se muestra la dependencia de la presión de vapor
de vapor obedecen a la ley de total (P T ) en una disolución de benceno-tolueno con la composición de la disolución.
Raoult.
Observe que sólo necesitamos expresar la composición de la disolución en términos de la
fracción molar de uno de los componentes. Para cada valor de X benceno , la fracción molar
del tolueno, X tolueno , está dada por (1 2 X benceno ). La disolución de benceno-tolueno cons-
tituye uno de los pocos ejemplos de una disolución ideal , que es cualquier disolución que
obedece la ley de Raoult. Una característica de una disolución ideal es que el calor de
disolución, DH disol , es cero.
La mayor parte de las disoluciones no se comporta de manera ideal en este aspecto.
Se consideran los siguientes dos casos, al designar dos sustancias volátiles como A y B:
Caso 1: Si las fuerzas intermoleculares entre las moléculas A y B son más débiles
que las fuerzas entre las moléculas de A y las fuerzas entre las moléculas de B, entonces
estas moléculas tienen mayor tendencia a abandonar la disolución que en el caso de una
disolución ideal. Como consecuencia, la presión de vapor de la disolución es mayor que
la suma de las presiones de vapor predicha por la ley de Raoult para la misma concentra-
ción. Este comportamiento da lugar a una desviación positiva [fi gura 12.8a)]. En este
caso, el calor de disolución es positivo (es decir, el proceso de mezclado es endotérmico).
Caso 2: Si las moléculas de A atraen las moléculas de B con más fuerza que las de
su misma clase, la presión de vapor de la disolución es menor que la suma de las presio-
Figura 12.8 Disoluciones no
ideales. a) La desviación positiva se
P
presenta cuando P T es mayor que T
la presión que predice la ley de P T
Raoult (la línea negra sólida). b)
Desviación negativa. En este caso
P T es menor que la presión que P P P
predice la ley de Raoult (línea negra Presión A Presión A B
sólida).
P B
0 0.2 0.4 0.6 0.8 1.0 0 0.2 0.4 0.6 0.8 1.0
X A X A
a) b)