Page 632 - Quimica - Undécima Edición
P. 632
602 CAPÍTULO 13 Cinética química
En la preparación de oxígeno molecular en el laboratorio, se calienta una muestra de
clorato de potasio, como se muestra en la fi gura 4.13b). La reacción es
2KClO 3 (s) ¡ 2KCl(s) 1 3O 2 (g)
Sin embargo, este proceso de descomposición térmica es muy lento en ausencia de un
catalizador. La rapidez de descomposición puede aumentarse drásticamente agregando una
pequeña cantidad del catalizador dióxido de manganeso(IV) (MnO 2 ) , un polvo de color
negro. Al fi nal de la reacción es posible recuperar todo el MnO 2 , de la misma manera que
2
todos los iones I permanecen después de la descomposición del H 2 O 2 .
Para ampliar la analogía del tránsito, la Un catalizador acelera una reacción al proporcionar una serie de etapas elementales
adición de un catalizador puede com-
pararse con la construcción de un tú- con cinéticas más favorables que las que existen en su ausencia. A partir de la ecuación
nel a través de una montaña para (13.11) sabemos que la constante de rapidez k (y, por lo tanto, la rapidez) de una reacción
comunicar dos poblaciones que antes depende del factor de frecuencia A y de la energía de activación E a ; cuanto mayor sea A,
estaban unidas por medio de una ca-
rretera tortuosa sobre la montaña. o menor E a , mayor será la rapidez. En muchos casos, un catalizador aumenta la rapidez
disminuyendo la energía de activación de una reacción.
Supongamos que la siguiente reacción tiene cierta constante de rapidez k y una ener-
gía de activación E a .
k
A 1 B ¡ C 1 D
En presencia de un catalizador, no obstante, la constante de rapidez es k c (denominada
constante de rapidez catalítica ):
k c
A 1 B ¡ C 1 D
A partir de la defi nición de un catalizador,
rapidez catalizada . rapidez sin catalizar
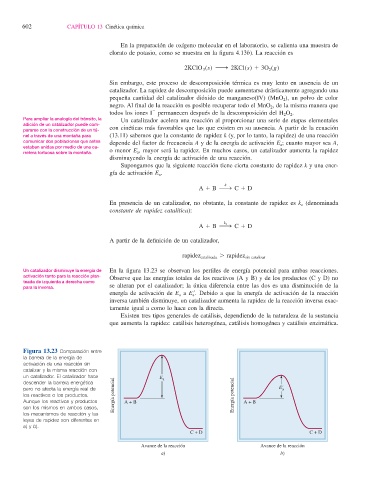
Un catalizador disminuye la energía de En la fi gura 13.23 se observan los perfi les de energía potencial para ambas reacciones.
activación tanto para la reacción plan- Observe que las energías totales de los reactivos (A y B) y de los productos (C y D) no
teada de izquierda a derecha como
para la inversa. se alteran por el catalizador; la única diferencia entre las dos es una disminución de la
energía de activación de E a a E a 9. Debido a que la energía de activación de la reacción
inversa también disminuye, un catalizador aumenta la rapidez de la reacción inversa exac-
tamente igual a como lo hace con la directa.
Existen tres tipos generales de catálisis , dependiendo de la naturaleza de la sustancia
que aumenta la rapidez: catálisis heterogénea , catálisis homogénea y catálisis enzimática .
Figura 13.23 Comparación entre
la barrera de la energía de
activación de una reacción sin
catalizar y la misma reacción con
un catalizador. El catalizador hace E a
descender la barrera energética
pero no afecta la energía real de E' a
los reactivos o los productos. Energía potencial Energía potencial
Aunque los reactivos y productos A + B A + B
son los mismos en ambos casos,
los mecanismos de reacción y las
leyes de rapidez son diferentes en
a) y b).
C + D C + D
Avance de la reacción Avance de la reacción
a) b)