Page 533 - Quimica - Undécima Edición
P. 533
11.8 Cambios de fase 503
Vapor
Punto de ebullición
Temperatura C Líquido y vapor D
en equilibrio
Punto de fusión
Líquido
Sólido y líquido
en equilibrio
A B
Sólido
Tiempo
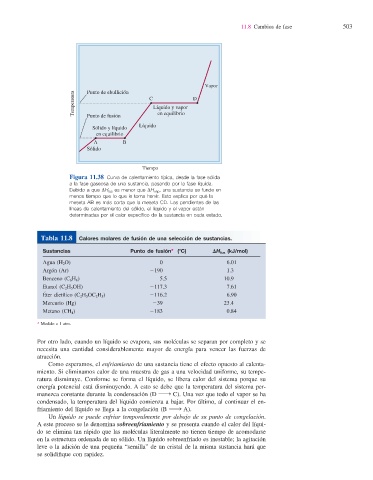
Figura 11.38 Curva de calentamiento típica, desde la fase sólida
a la fase gaseosa de una sustancia, pasando por la fase líquida.
Debido a que DH fus es menor que DH vap , una sustancia se funde en
menos tiempo que lo que le toma hervir. Esto explica por qué la
meseta AB es más corta que la meseta CD. Las pendientes de las
líneas de calentamiento del sólido, el líquido y el vapor están
determinadas por el calor específi co de la sustancia en cada estado.
Tabla 11.8 Calores molares de fusión de una selección de sustancias.
Sustancias Punto de fusión* (8C) DH fus (kJ/mol)
Agua (H 2 O) 0 6.01
Argón (Ar) 2190 1.3
Benceno (C 6 H 6 ) 5.5 10.9
Etanol (C 2 H 5 OH) 2117.3 7.61
Éter dietílico (C 2 H 5 OC 2 H 5 ) 2116.2 6.90
Mercurio (Hg) 239 23.4
Metano (CH 4 ) 2183 0.84
* Medido a 1 atm.
Por otro lado, cuando un líquido se evapora, sus moléculas se separan por completo y se
necesita una cantidad considerablemente mayor de energía para vencer las fuerzas de
atracción.
Como esperamos, el enfriamiento de una sustancia tiene el efecto opuesto al calenta-
miento. Si eliminamos calor de una muestra de gas a una velocidad uniforme, su tempe-
ratura disminuye. Conforme se forma el líquido, se libera calor del sistema porque su
energía potencial está disminuyendo. A esto se debe que la temperatura del sistema per-
manezca constante durante la condensación (D ¡ C). Una vez que todo el vapor se ha
condensado, la temperatura del líquido comienza a bajar. Por último, al continuar el en-
friamiento del líquido se llega a la congelación (B ¡ A).
Un líquido se puede enfriar temporalmente por debajo de su punto de congelación.
A este proceso se le denomina sobreenfriamiento y se presenta cuando el calor del líqui-
do se elimina tan rápido que las moléculas literalmente no tienen tiempo de acomodarse
en la estructura ordenada de un sólido. Un líquido sobreenfriado es inestable; la agitación
leve o la adición de una pequeña “semilla” de un cristal de la misma sustancia hará que
se solidifi que con rapidez.