Page 532 - Quimica - Undécima Edición
P. 532
502 CAPÍTULO 11 Fuerzas intermoleculares y líquidos y sólidos
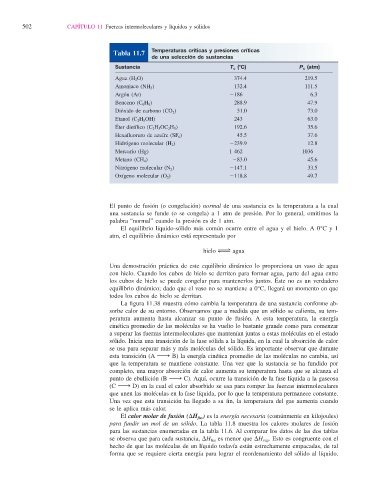
Temperaturas críticas y presiones críticas
Tabla 11.7
de una selección de sustancias
Sustancia T c (8C) P c (atm)
Agua (H 2 O) 374.4 219.5
Amoniaco (NH 3 ) 132.4 111.5
Argón (Ar) 2186 6.3
Benceno (C 6 H 6 ) 288.9 47.9
Dióxido de carbono (CO 2 ) 31.0 73.0
Etanol (C 2 H 5 OH) 243 63.0
Éter dietílico (C 2 H 5 OC 2 H 5 ) 192.6 35.6
Hexafl uoruro de azufre (SF 6 ) 45.5 37.6
Hidrógeno molecular (H 2 ) 2239.9 12.8
Mercurio (Hg) 1 462 1036
Metano (CH 4 ) 283.0 45.6
Nitrógeno molecular (N 2 ) 2147.1 33.5
Oxígeno molecular (O 2 ) 2118.8 49.7
El punto de fusión (o congelación) normal de una sustancia es la temperatura a la cual
una sustancia se funde (o se congela) a 1 atm de presión. Por lo general, omitimos la
palabra “normal” cuando la presión es de 1 atm.
El equilibrio líquido-sólido más común ocurre entre el agua y el hielo. A 0°C y 1
atm, el equilibrio dinámico está representado por
hielo Δ agua
Una demostración práctica de este equilibrio dinámico lo proporciona un vaso de agua
con hielo. Cuando los cubos de hielo se derriten para formar agua, parte del agua entre
los cubos de hielo se puede congelar para mantenerlos juntos. Éste no es un verdadero
equilibrio dinámico; dado que el vaso no se mantiene a 0°C, llegará un momento en que
todos los cubos de hielo se derritan.
La fi gura 11.38 muestra cómo cambia la temperatura de una sustancia conforme ab-
sorbe calor de su entorno. Observamos que a medida que un sólido se calienta, su tem-
peratura aumenta hasta alcanzar su punto de fusión. A esta temperatura, la energía
cinética promedio de las moléculas se ha vuelto lo bastante grande como para comenzar
a superar las fuerzas intermoleculares que mantenían juntas a estas moléculas en el estado
sólido. Inicia una transición de la fase sólida a la líquida , en la cual la absorción de calor
se usa para separar más y más moléculas del sólido. Es importante observar que durante
esta transición (A ¡ B) la energía cinética promedio de las moléculas no cambia, así
que la temperatura se mantiene constante. Una vez que la sustancia se ha fundido por
completo, una mayor absorción de calor aumenta su temperatura hasta que se alcanza el
punto de ebullición (B ¡ C). Aquí, ocurre la transición de la fase líquida a la gaseosa
(C ¡ D) en la cual el calor absorbido se usa para romper las fuerzas intermoleculares
que unen las moléculas en la fase líquida, por lo que la temperatura permanece constante.
Una vez que esta transición ha llegado a su fi n, la temperatura del gas aumenta cuando
se le aplica más calor.
El calor molar de fusión (DH fus ) es la energía necesaria (comúnmente en kilojoules)
para fundir un mol de un sólido. La tabla 11.8 muestra los calores molares de fusión
para las sustancias enumeradas en la tabla 11.6. Al comparar los datos de las dos tablas
se observa que para cada sustancia, DH fus es menor que DH vap . Esto es congruente con el
hecho de que las moléculas de un líquido todavía están estrechamente empacadas, de tal
forma que se requiere cierta energía para lograr el reordenamiento del sólido al líquido.