Page 527 - Quimica - Undécima Edición
P. 527
11.8 Cambios de fase 497
¿Qué sucede a nivel molecular durante la evaporación? Al principio, el tráfi co es en
un solo sentido: las moléculas se desplazan desde el líquido hacia el espacio vacío. En
cuanto las moléculas dejan el líquido, establecen una fase de vapor. Cuando aumenta la
concentración de las moléculas en la fase de vapor, algunas se condensan, es decir, regre-
san a la fase líquida. El proceso de condensación , o el cambio de la fase gaseosa a la
fase líquida, ocurre cuando una molécula choca en la superfi cie del líquido y queda atra-
pada por las fuerzas intermoleculares del líquido .
La velocidad de evaporación es constante a una temperatura dada y la velocidad de
La presión de vapor de equilibrio es
condensación aumenta con el incremento de la concentración de las moléculas en la fase independiente de la cantidad de
de vapor. En cierto momento se llega a un estado de equilibrio dinámico , cuando la ve- líquido siempre que haya algo de lí-
locidad del proceso en un sentido está exactamente balanceada por la velocidad del quido presente.
proceso inverso, es decir, cuando las velocidades de condensación y evaporación se igua-
lan (fi gura 11.34). La presión de vapor de equilibrio es la presión de vapor medida Animación
cuando hay un equilibrio dinámico entre la condensación y la evaporación. Con frecuen- Presión de vapor de equilibrio
cia, sólo se emplea el término “presión de vapor” para describir la presión de vapor de
equilibrio de un líquido . Este término es aceptable en tanto se conozca el signifi cado del
Animación
término abreviado. Equilibrio dinámico
Es importante observar que la presión de vapor de equilibrio es la máxima presión
de vapor de un líquido a una temperatura dada y que permanece constante a temperatura
constante. (Es independiente de la cantidad de líquido siempre y cuando haya un poco de
líquido presente.) De aquí se desprende que la presión de vapor de un líquido aumenta
con la temperatura. Las gráfi cas de presión de vapor en función de la temperatura para
tres líquidos distintos que aparecen en la fi gura 11.35 lo confi rman. Rapidez de Equilibrio
evaporación dinámico
Rapidez establecido
Calor molar de vaporización y punto de ebullición
El calor molar de vaporización (DH vap ) es una medida de la intensidad de las fuerzas
Rapidez de
intermoleculares que se ejercen en un líquido. Esta propiedad se defi ne como la energía
condensación
(por lo general en kilojoules) necesaria para evaporar un mol de un líquido. El calor
molar de vaporización está relacionado directamente con la magnitud de las fuerzas inter-
Tiempo
moleculares que hay en el líquido. Si la atracción intermolecular es fuerte, se necesita
mucha energía para liberar las moléculas de la fase líquida. En consecuencia, el líquido Figura 11.34 Comparación de
las rapideces de evaporación y
tiene una presión de vapor relativamente baja y un elevado calor molar de vaporización.
condensación conforme el sistema
El análisis previo predice que la presión de vapor de equilibrio (P) de un líquido tiende al equilibrio a temperatura
debería incrementarse con el aumento de temperatura, como se muestra en la fi gura 11.35. constante.
2 Éter dietílico Agua Mercurio
Presión de vapor (atm) 1
–100 0 34.6 100 200 357 400
Temperatura (°C)
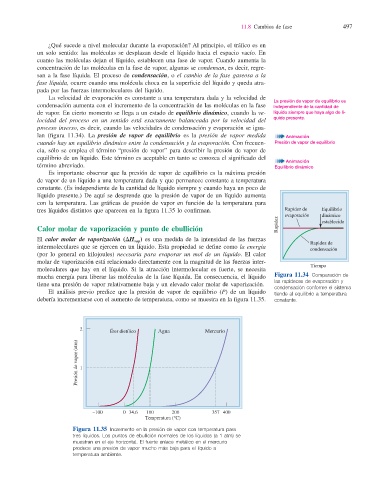
Figura 11.35 Incremento en la presión de vapor con temperatura para
tres líquidos. Los puntos de ebullición normales de los líquidos (a 1 atm) se
muestran en el eje horizontal. El fuerte enlace metálico en el mercurio
produce una presión de vapor mucho más baja para el líquido a
temperatura ambiente.