Page 534 - Quimica - Undécima Edición
P. 534
504 CAPÍTULO 11 Fuerzas intermoleculares y líquidos y sólidos
Equilibrio sólido-vapor
Los sólidos también experimentan evaporación y, por consiguiente, poseen una presión de
vapor. Considere el siguiente equilibrio dinámico:
sólido Δ vapor
El proceso en el cual las moléculas pasan directamente de sólido a vapor se conoce como
sublimación . El proceso inverso se denomina deposición , es decir, las moléculas hacen la
transición directa de vapor a sólido. El naftaleno , la sustancia con la que se fabrican bo-
litas para combatir la polilla, tiene una presión de vapor (de equilibrio) bastante alta para
un sólido (1 mmHg a 53°C); por ello, su vapor picante impregna muy rápido un espacio
cerrado. El yodo también sublima. Arriba de la temperatura ambiente, el color violeta del
vapor del yodo es fácilmente visible en un recipiente cerrado.
Como las moléculas están unidas con más fuerza en un sólido, su presión de vapor
suele ser mucho menor que la del líquido correspondiente. La energía (por lo general en
kilojoules) necesaria para sublimar un mol de un sólido recibe el nombre de calor molar
de sublimación (DH sub ) , y es igual a la suma de los calores molares de fusión y vapori-
zación:
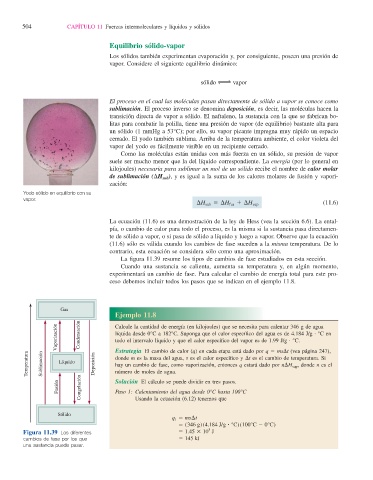
Yodo sólido en equilibrio con su
vapor.
DH sub 5 DH fus 1 DH vap (11.6)
La ecuación (11.6) es una demostración de la ley de Hess (vea la sección 6.6). La ental-
pía , o cambio de calor para todo el proceso, es la misma si la sustancia pasa directamen-
te de sólido a vapor, o si pasa de sólido a líquido y luego a vapor. Observe que la ecuación
(11.6) sólo es válida cuando los cambios de fase suceden a la misma temperatura. De lo
contrario, esta ecuación se considera sólo como una aproximación.
La fi gura 11.39 resume los tipos de cambios de fase estudiados en esta sección.
Cuando una sustancia se calienta, aumenta su temperatura y, en algún momento,
experimentará un cambio de fase. Para calcular el cambio de energía total para este pro-
ceso debemos incluir todos los pasos que se indican en el ejemplo 11.8.
Gas
Ejemplo 11.8
Vaporización Condensación Calcule la cantidad de energía (en kilojoules) que se necesita para calentar 346 g de agua
líquida desde 0°C a 182°C. Suponga que el calor específi co del agua es de 4.184 J/g · °C en
todo el intervalo líquido y que el calor específi co del vapor es de 1.99 J/g · °C.
Temperatura Sublimación Líquido Deposición Estrategia El cambio de calor (q) en cada etapa está dado por q 5 msDt (vea página 247),
donde m es la masa del agua, s es el calor específi co y Dt es el cambio de temperatura. Si
hay un cambio de fase, como vaporización, entonces q estará dado por nDH vap , donde n es el
número de moles de agua.
Fusión Congelación Solución El cálculo se puede dividir en tres pasos.
Paso 1: Calentamiento del agua desde 0°C hasta 100°C
Usando la ecuación (6.12) tenemos que
Sólido
q 1 5 ms¢t
5 (346 g)(4.184 J/g ? °C)(100°C 2 0°C)
5
Figura 11.39 Los diferentes 5 1.45 3 10 J
cambios de fase por los que 5 145 kJ
una sustancia puede pasar.