Page 314 - Fisica General Burbano
P. 314
LICUEFACCIÓN DE GASES. ECUACIÓN DE VAN DER WAALS 325
vapor es la tensión máxima. (Rama 2 paralela al eje V). Licuado todo el vapor, a grandes aumen-
tos de presión corresponden pequeñas variaciones de volumen por la poca compresibilidad de los
líquidos. (Rama 3 del gráfico).
XV 31. Isotermas de los gases reales. Punto crítico
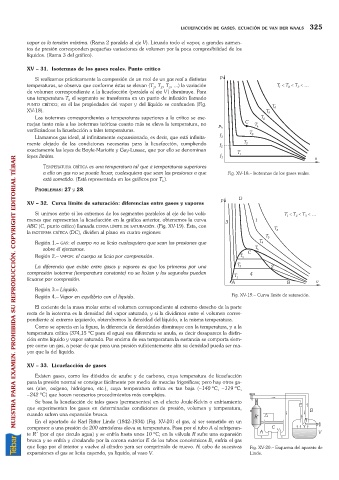
Si realizamos prácticamente la compresión de un mol de un gas real a distintas
temperaturas, se observa que conforme éstas se elevan (T , T , T , ...) la variación
1
2
3
de volumen correspondiente a la licuefacción (paralela al eje V) disminuye. Para
una temperatura T el segmento se transforma en un punto de inflexión llamado
k
PUNTO CRÍTICO; en él las propiedades del vapor y del líquido se confunden (Fig.
XV-18).
Las isotermas correspondientes a temperaturas superiores a la crítica se ase-
mejan tanto más a las isotermas teóricas cuanto más se eleva la temperatura, no
verificándose la licuefacción a tales temperaturas.
Llamamos gas ideal, al infinitamente expansionado, es decir, que está infinita-
mente alejado de las condiciones necesarias para la licuefacción, cumpliendo
exactamente las leyes de Boyle-Mariotte y Gay-Lussac, que por ello se denominan
leyes límites.
MUESTRA PARA EXAMEN. PROHIBIDA SU REPRODUCCIÓN. COPYRIGHT EDITORIAL TÉBAR
TEMPERATURA CRÍTICA es una temperatura tal que a temperaturas superiores
a ella un gas no se puede licuar, cualesquiera que sean las presiones a que Fig. XV-18. Isotermas de los gases reales.
está sometido. (Está representada en los gráficos por T ).
k
PROBLEMAS:27 y 28.
XV 32. Curva límite de saturación: diferencias entre gases y vapores
Si unimos entre sí los extremos de los segmentos paralelos al eje de los volú-
menes que representan la licuefacción en la gráfica anterior, obtenemos la curva
ABC (C, punto crítico) llamada CURVA LÍMITE DE SATURACIÓN. (Fig. XV-19). Ésta, con
la ISOTERMA CRÍTICA (DC), dividen al plano en cuatro regiones:
Región 1. GAS: el cuerpo no se licúa cualesquiera que sean las presiones que
sobre él ejerzamos.
Región 2. VAPOR: el cuerpo se licúa por comprensión.
La diferencia que existe entre gases y vapores es que los primeros por una
compresión isoterma (temperatura constante) no se licúan y los segundos pueden
licuarse por compresión.
Región 3. Líquido.
Región 4. Vapor en equilibrio con el líquido. Fig. XV-19. Curva límite de saturación.
El cociente de la masa molar entre el volumen correspondiente al extremo derecho de la parte
recta de la isoterma es la densidad del vapor saturado, y si la dividimos entre el volumen corres-
pondiente al extremo izquierdo, obtendremos la densidad del líquido, a la misma temperatura.
Como se aprecia en la figura, la diferencia de densidades disminuye con la temperatura, y a la
temperatura crítica (374,15 ºC para el agua) esa diferencia se anula, es decir desaparece la distin-
ción entre líquido y vapor saturado. Por encima de esa temperatura la sustancia se comporta siem-
pre como un gas, a pesar de que para una presión suficientemente alta su densidad pueda ser ma-
yor que la del líquido.
XV 33. Licuefacción de gases
Existen gases, como los dióxidos de azufre y de carbono, cuya temperatura de licuefacción
para la presión normal se consigue fácilmente por medio de mezclas frigoríficas; pero hay otros ga-
ses (aire, oxígeno, hidrógeno, etc.), cuya temperatura crítica es tan baja (140 ºC, 119 ºC,
242 ºC) que hacen necesarios procedimientos más complejos.
Se basa la licuefacción de tales gases (permanentes) en el efecto Joule-Kelvin o enfriamiento
que experimentan los gases en determinadas condiciones de presión, volumen y temperatura,
cuando sufren una expansión brusca.
En el apartado de Karl Ritter Linde (1842-1934) (Fig. XV-20) el gas, al ser sometido en un
compresor a una presión de 200 atmósferas eleva su temperatura. Pasa por el tubo A al refrigeran-
te R¢(por el que circula agua) y se enfría hasta unos 10 ºC; en la válvula R sufre una expansión
brusca y se enfría y circulando por la corona exterior E de los tubos concéntricos B, enfría el gas
que llega por el interior y vuelve al cilindro para ser comprimido de nuevo. Al cabo de sucesivas Fig. XV-20. Esquema del aparato de
expansiones el gas se licúa cayendo, ya líquido, al vaso V. Linde.