Page 652 - Quimica - Undécima Edición
P. 652
622 CAPÍTULO 13 Cinética química
3
peratura se contamina con 2.0 ppm de NO por volumen. reacción se ha estimado en 6.4 3 10 min. ¿Cuál sería
Bajo estas condiciones, ¿se puede simplifi car la ley de la media vida si la concentración inicial de NO fuera de
rapidez? Si es así, escriba la ley de rapidez simplifi cada. 10 ppm?
c) Bajo la condición descrita en b), la media vida de la
Interpretación, modelación y estimación
13.137 Un instructor realizó una demostración en clase de la 13.141 ¿Cuáles son los tiempos más cortos y los más largos (en
reacción termita (vea la página 259). Mezcló aluminio años) que se pueden estimar por datación con carbo-
con óxido de hierro(III) en una cubeta metálica colocada no-14?
en un cubo de hielo. Después de que comenzó la reac- 13.142 Además de los sistemas químicos y biológicos, algunas
ción extremadamente exotérmica, hubo un enorme esta- veces se pueden aplicar tratamientos cinéticos a proce-
llido que no era característico de las reacciones termita. sos conductuales y sociales como la evolución de la
Dé una explicación química factible para el inesperado tecnología. Por ejemplo, en 1965, Gordon Moore,
efecto de sonido. La cubeta estaba abierta al aire. cofundador de Intel, describió una tendencia de que el
13.138 Tomando en cuenta la variación de la rapidez de una número de transistores en un circuito integrado (N) se
reacción catalizada por enzimas contra temperatura que duplica aproximadamente cada 1.5 años. Ahora llama-
se muestra aquí, ¿cuál es la temperatura aproximada que da ley de Moore, esta tendencia ha persistido durante
corresponde a la máxima rapidez en el cuerpo humano? las últimas décadas. Aquí se muestra una gráfi ca de ln
N contra años. a) Determine la constante de rapidez
para el crecimiento en el número de transistores en un
circuito integrado. b) Con base en la constante de rapi-
Rapidez dez, ¿cuánto tiempo se necesita para que N se duplique?
Si la ley de Moore continúa hasta el fi nal del siglo, ¿cuál
será el número de transistores en un circuito integrado
en el año 2100? Comente sobre su resultado.
25
T
20
13.139 ¿La constante de velocidad (k) de una reacción es más
sensible a cambios en la temperatura si E a es pequeña o ln N t 15
si es grande? 10
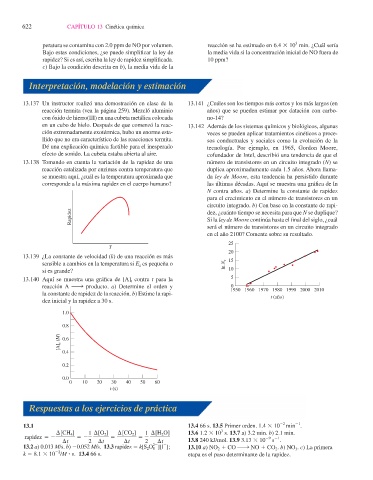
13.140 Aquí se muestra una gráfi ca de [A] t contra t para la 5
reacción A ¡ producto. a) Determine el orden y 0
1950 1960 1970 1980 1990 2000 2010
la constante de rapidez de la reacción. b) Estime la rapi-
t (año)
dez inicial y la rapidez a 30 s.
1.0
0.8
[A] t (M) 0.6
0.4
0.2
0.0
0 10 20 30 40 50 60
t (s)
Respuestas a los ejercicios de práctica
21
13.1 13.4 66 s. 13.5 Primer orden. 1.4 3 10 22 min .
3
¢[CH 4 ] 1 ¢[O 2 ] ¢[CO 2 ] 1 ¢[H 2 O] 13.6 1.2 3 10 s. 13.7 a) 3.2 min. b) 2.1 min.
rapidez 52 52 5 5 29 21
¢t 2 ¢t ¢t 2 ¢t 13.8 240 kJ/mol. 13.9 3.13 3 10 s .
2
22
13.2 a) 0.013 M/s. b) 20.052 M/s. 13.3 rapidez 5 k[S 2 O 8 ][I ]; 13.10 a) NO 2 1 CO ¡ NO 1 CO 2 . b) NO 3 . c) La primera
22
k 5 8.1 3 10 /M ? s. 13.4 66 s. etapa es el paso determinante de la rapidez.