Page 650 - Quimica - Undécima Edición
P. 650
620 CAPÍTULO 13 Cinética química
términos generales, las reacciones tienen los mismos donde la constante de rapidez de segundo orden es de
6
factores de frecuencia. 2.1 3 10 /M ? s a 37°C. (La reacción es de primer
orden en Hb y O 2 .) Para un adulto promedio, las con-
Energía potencial 50 kJ/mol 40 kJ/mol son de 8.0 3 10 M y 1.5 3 10 M, respectivamente.
20 kJ/mol
centraciones de Hb y O 2 en la sangre de los pulmones
30 kJ/mol
26
26
a) Calcule la rapidez de formación de HbO 2 . b) Calcule
la rapidez de consumo de O 2 . c) La rapidez de forma-
24
ción de HbO 2 se incrementa a 1.4 3 10 M/s durante
20 kJ/mol
40 kJ/mol
el ejercicio para satisfacer la demanda de la rapidez
Avance de la reacción Avance de la reacción Avance de la reacción
incrementada del metabolismo. Si se supone que la
a) b) c)
concentración de Hb se mantiene igual, ¿cuál será
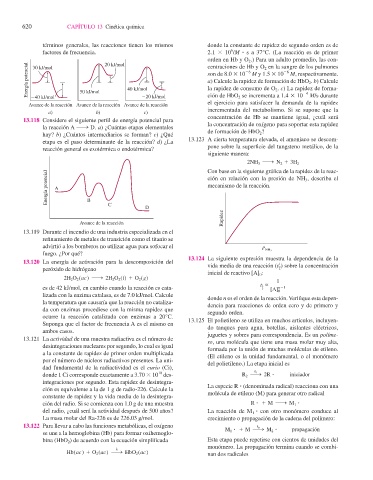
13.118 Considere el siguiente perfi l de energía potencial para
la concentración de oxígeno para soportar esta rapidez
la reacción A ¡ D. a) ¿Cuántas etapas elementales
hay? b) ¿Cuántos intermediarios se forman? c) ¿Qué de formación de HbO 2 ?
13.123 A cierta temperatura elevada, el amoniaco se descom-
etapa es el paso determinante de la reacción? d) ¿La
reacción general es exotérmica o endotérmica? pone sobre la superfi cie del tungsteno metálico, de la
siguiente manera:
2NH 3 ¡ N 2 1 3H 2
Con base en la siguiente gráfi ca de la rapidez de la reac-
Energía potencial A ción en relación con la presión de NH 3 , describa el
mecanismo de la reacción.
B
C
D
Rapidez
Avance de la reacción
13.119 Durante el incendio de una industria especializada en el
refi namiento de metales de transición como el titanio se
advirtió a los bomberos no utilizar agua para sofocar el
P NH 3
fuego. ¿Por qué?
13.124 La siguiente expresión muestra la dependencia de la
13.120 La energía de activación para la descomposición del 1
peróxido de hidrógeno vida media de una reacción (t ) sobre la concentración
2
inicial de reactivo [A] 0 :
2H 2 O 2 (ac) ¡ 2H 2 O 2 (l) 1 O 2 (g)
1
t1 ~
es de 42 kJ/mol, en cambio cuando la reacción es cata- 2 n21
[A] 0
lizada con la enzima catalasa, es de 7.0 kJ/mol. Calcule donde n es el orden de la reacción. Verifi que esta depen-
la temperatura que causaría que la reacción no cataliza-
dencia para reacciones de orden cero y de primero y
da con enzimas procediese con la misma rapidez que segundo orden.
ocurre la reacción catalizada con enzimas a 20°C.
13.125 El polietileno se utiliza en muchos artículos, incluyen-
Suponga que el factor de frecuencia A es el mismo en
ambos casos. do tanques para agua, botellas, aislantes eléctricos,
juguetes y sobres para correspondencia. Es un políme-
13.121 La actividad de una muestra radiactiva es el número de ro, una molécula que tiene una masa molar muy alta,
desintegraciones nucleares por segundo, lo cual es igual
formada por la unión de muchas moléculas de etileno.
a la constante de rapidez de primer orden multiplicada (El etileno es la unidad fundamental, o el monómero
por el número de núcleos radiactivos presentes. La uni-
del polietileno.) La etapa inicial es
dad fundamental de la radiactividad es el curio (Ci),
10
k 1
donde 1 Ci corresponde exactamente a 3.70 3 10 des- R 2 ¡ 2R ? iniciador
integraciones por segundo. Esta rapidez de desintegra-
ción es equivalente a la de 1 g de radio-226. Calcule la La especie R ? (denominada radical) reacciona con una
molécula de etileno (M) para generar otro radical
constante de rapidez y la vida media de la desintegra-
ción del radio. Si se comienza con 1.0 g de una muestra R ? 1 M ¡ M 1 ?
del radio, ¿cuál será la actividad después de 500 años? La reacción de M 1 ? con otro monómero conduce al
La masa molar del Ra-226 es de 226.03 g/mol. crecimiento o propagación de la cadena del polímero:
13.122 Para llevar a cabo las funciones metabólicas, el oxígeno M 1 ? 1 M ¡ M 2 ? propagación
k p
se une a la hemoglobina (Hb) para formar oxihemoglo-
bina (HbO 2 ) de acuerdo con la ecuación simplifi cada Esta etapa puede repetirse con cientos de unidades del
monómero. La propagación termina cuando se combi-
k
Hb(ac) 1 O 2 (ac) ¡ HbO 2 (ac) nan dos radicales