Page 647 - Quimica - Undécima Edición
P. 647
Preguntas y problemas 617
22
2
22
13.81 La reacción procede
S 2 O 8 1 2I ¡ 2SO 4 1 I 2
lentamente en disolución acuosa, pero puede ser catali-
31
2
31
zada por el ion Fe . Puesto que el Fe oxida el I y el
22
21
Fe reduce el S 2 O 8 , escriba un mecanismo factible de III
dos etapas para esta reacción. Explique por qué la reac-
ción sin catálisis es tan lenta.
13.82 ¿Cuáles son las unidades de la constante de rapidez t 5 0 s t 5 50 s
para una reacción de tercer orden?
13.87 Con referencia al ejemplo 13.5, explique cómo se
13.83 La ley de rapidez integrada para una reacción de orden
mediría experimentalmente la presión parcial del azo-
cero A ¡ B es [A] t 5 [A] 0 2 kt. a) Trace las siguien- metano en función del tiempo.
tes gráfi cas: i) rapidez contra [A] t y ii) [A] t contra t. b)
13.88 La ley de rapidez para la reacción 2NO 2 (g) ¡
Derive una expresión para la vida media de la reacción. N 2 O 4 (g) es rapidez 5 k[NO 2 ] . ¿Cuál de los siguientes
2
c) Calcule el tiempo expresado en vidas medias cuando
cambios provocará un cambio en el valor de k? a) La
la ley de rapidez integrada ya no es válida, es decir, presión de NO 2 se duplica. b) La reacción se lleva a
cuando [A] t 5 0.
cabo en un disolvente orgánico. c) El volumen del reci-
13.84 Un matraz contiene una mezcla de los compuestos A y piente se duplica. d) Se disminuye la temperatura. e) Se
B. Ambos compuestos se descomponen siguiendo una añade un catalizador al recipiente.
cinética de primer orden. La vida media es de 50.0 min 13.89 La reacción de G 2 con E 2 para formar 2EG es exotérmi-
para A y de 18.0 min para B. Si las concentraciones de
ca, y la reacción de G 2 con X 2 para formar 2XG es
A y B son iguales al inicio, ¿cuánto tiempo transcurrirá endotérmica. La energía de activación de la reacción
para que la concentración de A sea cuatro veces la de
exotérmica es mayor que la de la reacción endotérmica.
B? Trace un diagrama del perfi l de la energía potencial
13.85 Aquí se muestran gráfi cas de concentración de reactivo para estas dos reacciones, en la misma gráfi ca.
contra tiempo para dos reacciones de primer orden a la 13.90 En la industria nuclear, los trabajadores utilizan como
misma temperatura. En cada caso, determine cuál reac- regla de oro que la radiactividad de cualquier muestra
ción tiene una mayor constante de rapidez. es inofensiva después de diez vidas medias. Calcule la
fracción de una muestra radiactiva que permanece des-
pués de este periodo. (Sugerencia: La desintegración
radiactiva sigue una cinética de primer orden.)
ln [A] t zador en cada uno de los siguientes aspectos: a) energía
[A] 13.91 Haga un comentario breve sobre el efecto de un catali-
t
de activación, b) mecanismo de reacción, c) entalpía de
la reacción, d) rapidez de una etapa en el sentido de
izquierda a derecha de una ecuación química, e) rapi-
t t
dez de una etapa en el sentido de derecha a izquierda de
a) b)
una ecuación química.
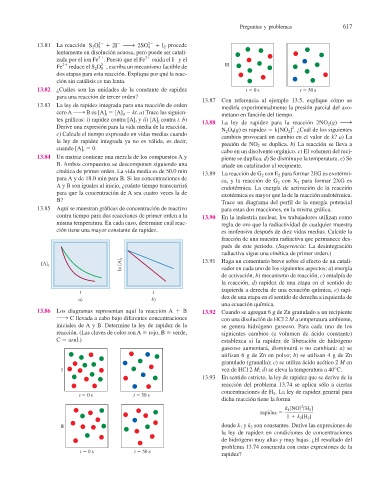
13.86 Los diagramas representan aquí la reacción A 1 B 13.92 Cuando se agregan 6 g de Zn granulado a un recipiente
¡ C llevada a cabo bajo diferentes concentraciones con una disolución de HCl 2 M a temperatura ambiente,
iniciales de A y B. Determine la ley de rapidez de la se genera hidrógeno gaseoso. Para cada uno de los
reacción. (Las claves de color son A 5 rojo, B 5 verde, siguientes cambios (a volumen de ácido constante)
C 5 azul.) establezca si la rapidez de liberación de hidrógeno
gaseoso aumentará, disminuirá o no cambiará: a) se
utilizan 6 g de Zn en polvo; b) se utilizan 4 g de Zn
granulado (granalla); c) se utiliza ácido acético 2 M en
I vez de HCl 2 M; d) se eleva la temperatura a 40°C.
13.93 En sentido estricto, la ley de rapidez que se deriva de la
reacción del problema 13.74 se aplica sólo a ciertas
concentraciones de H 2 . La ley de rapidez general para
t 5 0 s t 5 50 s
dicha reacción tiene la forma
2
k 1 [NO] [H 2 ]
rapidez 5
1 1 k 2 [H 2 ]
II donde k 1 y k 2 son constantes. Derive las expresiones de
la ley de rapidez en condiciones de concentraciones
de hidrógeno muy altas y muy bajas. ¿El resultado del
problema 13.74 concuerda con estas expresiones de la
t 5 0 s t 5 50 s
rapidez?