Page 643 - Quimica - Undécima Edición
P. 643
Preguntas y problemas 613
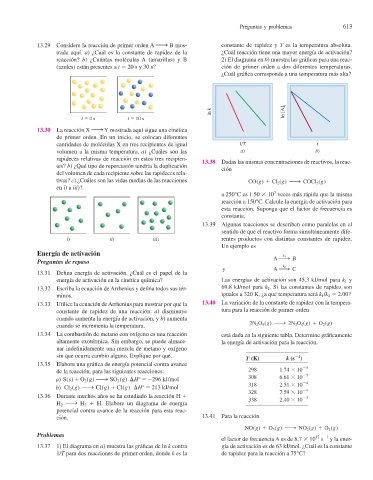
13.29 Considere la reacción de primer orden A ¡ B mos- constante de rapidez y T es la temperatura absoluta.
trada aquí. a) ¿Cuál es la constante de rapidez de la ¿Cuál reacción tiene una mayor energía de activación?
reacción? b) ¿Cuántas moléculas A (amarillas) y B 2) El diagrama en b) muestra las gráfi cas para una reac-
(azules) están presentes a t 5 20 s y 30 s? ción de primer orden a dos diferentes temperaturas.
¿Cuál gráfi ca corresponde a una temperatura más alta?
ln k ln [A] t
t 0 s t 10 s
13.30 La reacción X ¡ Y mostrada aquí sigue una cinética
de primer orden. En un inicio, se colocan diferentes
cantidades de moléculas X en tres recipientes de igual 1/T t
volumen a la misma temperatura. a) ¿Cuáles son las a) b)
rapideces relativas de reacción en estos tres recipien- 13.38 Dadas las mismas concentraciones de reactivos, la reac-
tes? b) ¿Qué tipo de repercusión tendría la duplicación
ción
del volumen de cada recipiente sobre las rapideces rela-
tivas? c) ¿Cuáles son las vidas medias de las reacciones CO(g) 1 Cl 2 (g) ¡ COCl 2 (g)
en i) a iii)?
3
a 250°C es 1.50 3 10 veces más rápida que la misma
reacción a 150°C. Calcule la energía de activación para
esta reacción. Suponga que el factor de frecuencia es
constante.
13.39 Algunas reacciones se describen como paralelas en el
sentido de que el reactivo forma simultáneamente dife-
i) ii) iii) rentes productos con distintas constantes de rapidez.
Un ejemplo es
Energía de activación k 1
A ¡ B
Preguntas de repaso
k 2
y A ¡ C
13.31 Defi na energía de activación. ¿Cuál es el papel de la
energía de activación en la cinética química? Las energías de activación son 45.3 kJ/mol para k 1 y
13.32 Escriba la ecuación de Arrhenius y defi na todos sus tér- 69.8 kJ/mol para k 2 . Si las constantes de rapidez son
minos. iguales a 320 K, ¿a qué temperatura será k 1 /k 2 5 2.00?
13.33 Utilice la ecuación de Arrhenius para mostrar por qué la 13.40 La variación de la constante de rapidez con la tempera-
constante de rapidez de una reacción: a) disminuye tura para la reacción de primer orden
cuando aumenta la energía de activación, y b) aumenta
2N 2 O 5 (g) ¡ 2N 2 O 4 (g) 1 O 2 (g)
cuando se incrementa la temperatura.
13.34 La combustión de metano con oxígeno es una reacción está dada en la siguiente tabla. Determine gráfi camente
altamente exotérmica. Sin embargo, se puede almace- la energía de activación para la reacción.
nar indefi nidamente una mezcla de metano y oxígeno
sin que ocurra cambio alguno. Explique por qué. 1
T (K) k (s )
13.35 Elabore una gráfi ca de energía potencial contra avance 5
de la reacción, para las siguientes reacciones: 298 1.74 10
a) S(s) 1O 2 (g) ¡ SO 2 (g) ¢H°52296 kJ/mol 308 6.61 10 5
318 2.51 10 4
b) Cl 2 (g) ¡ Cl(g) 1 Cl(g) ¢H° 5 243 kJ/mol
328 7.59 10 4
13.36 Durante muchos años se ha estudiado la reacción H 1 3
338 2.40 10
H 2 ¡ H 2 1 H. Elabore un diagrama de energía
potencial contra avance de la reacción para esta reac-
ción. 13.41 Para la reacción
NO(g) 1 O 3 (g) ¡ NO 2 (g) 1 O 2 (g)
Problemas 12 21
el factor de frecuencia A es de 8.7 3 10 s y la ener-
13.37 1) El diagrama en a) muestra las gráfi cas de ln k contra gía de activación es de 63 kJ/mol. ¿Cuál es la constante
1/T para dos reacciones de primer orden, donde k es la de rapidez para la reacción a 75°C?