Page 248 - Libro Hipertextos Fisica 1
P. 248
Calor y temperatura
n Relación entre el calor suministrado y la masa para un aumento
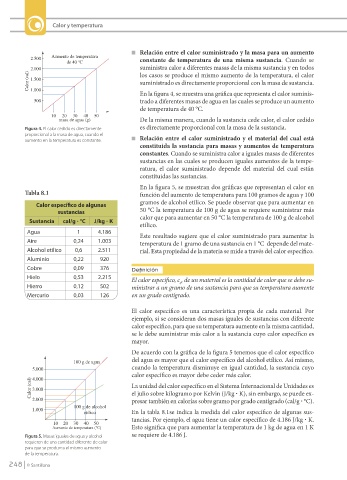
Aumento de temperatura
2.500 constante de temperatura de una misma sustancia. Cuando se
de 40 ºC
2.000 suministra calor a diferentes masas de la misma sustancia y en todos
los casos se produce el mismo aumento de la temperatura, el calor
Calor (cal) 1.500 suministrado es directamente proporcional con la masa de sustancia.
1.000
En la figura 4, se muestra una gráfica que representa el calor suminis-
500 trado a diferentes masas de agua en las cuales se produce un aumento
de temperatura de 40 °C.
10 20 30 40 50
masa de agua (g) De la misma manera, cuando la sustancia cede calor, el calor cedido
Figura 4. El calor cedido es directamente es directamente proporcional con la masa de la sustancia.
proporcional a la masa de agua, cuando el
aumento en la temperatura es constante. n Relación entre el calor suministrado y el material del cual está
constituida la sustancia para masas y aumentos de temperatura
constantes. Cuando se suministra calor a iguales masas de diferentes
sustancias en las cuales se producen iguales aumentos de la tempe-
ratura, el calor suministrado depende del material del cual están
constituidas las sustancias.
En la figura 5, se muestran dos gráficas que representan el calor en
Tabla 8.1 función del aumento de temperatura para 100 gramos de agua y 100
gramos de alcohol etílico. Se puede observar que para aumentar en
Calor específico de algunas
sustancias 50 °C la temperatura de 100 g de agua se requiere suministrar más
Sustancia cal/g ? °C J/kg ? K calor que para aumentar en 50 °C la temperatura de 100 g de alcohol
etílico.
Agua 1 4.186 Este resultado sugiere que el calor suministrado para aumentar la
Aire 0,24 1.003 temperatura de 1 gramo de una sustancia en 1 °C depende del mate-
Alcohol etílico 0,6 2.511 rial. Esta propiedad de la materia se mide a través del calor específico.
Aluminio 0,22 920
Cobre 0,09 376 Definición
Hielo 0,53 2.215 El calor específico, c , de un material es la cantidad de calor que se debe su-
e
Hierro 0,12 502 ministrar a un gramo de una sustancia para que su temperatura aumente
Mercurio 0,03 126 en un grado centígrado.
El calor específico es una característica propia de cada material. Por
ejemplo, si se consideran dos masas iguales de sustancias con diferente
calor específico, para que su temperatura aumente en la misma cantidad,
se le debe suministrar más calor a la sustancia cuyo calor específico es
mayor.
De acuerdo con la gráfica de la figura 5 tenemos que el calor específico
del agua es mayor que el calor específico del alcohol etílico. Así mismo,
100 g de agua
5.000 cuando la temperatura disminuye en igual cantidad, la sustancia cuyo
calor específico es mayor debe ceder más calor.
4.000
Calor (cal) 3.000 La unidad del calor específico en el Sistema Internacional de Unidades es
el julio sobre kilogramo por Kelvin (J/kg ? K), sin embargo, se puede ex-
2.000 presar también en calorías sobre gramo por grado centígrado (cal/g ? °C).
100 g de alcohol
1.000
etílico En la tabla 8.1se indica la medida del calor específico de algunas sus-
tancias. Por ejemplo, el agua tiene un calor específico de 4.186 J/kg ? K.
10 20 30 40 50
Aumento de temperatura (ºC) Esto significa que para aumentar la temperatura de 1 kg de agua en 1 K
Figura 5. Masas iguales de agua y alcohol se requiere de 4.186 J.
requieren de una cantidad diferente de calor
para que se produzca el mismo aumento
de la temperatura.
248 © Santillana
FI10-U8(242-273).indd 248 4/10/10 18:00